Тау протеини могу да предвиђају места дегенерације мозга у Алцхајмеровој болести
Снимање мозга тау-протеинских „заврзлама“ предвиђа локацију будуће атрофије мозга код пацијената са Алцхајмеровом болести годину дана или више унапред, према новој студији.
Супротно томе, утврђено је да локација амилоидних „плакова“, који су деценијама били у фокусу Алцхајмеровог истраживања и развоја лекова, није била од користи у предвиђању како ће се штета развијати како болест напредује, према научницима са Универзитета у Калифорнијски центар за памћење и старење у Сан Франциску.
Резултати подржавају све веће препознавање да тау дегенерацију мозга код Алзхеимерове болести води директније од амилоидног протеина, према истраживачима.
Такође демонстрира потенцијал недавно развијене технологије снимања мозга засноване на тау-бази позитронске емисионе томографије (ПЕТ) да би убрзала клиничка испитивања Алзхеимерове болести и побољшала индивидуалну негу пацијената, кажу они.
„Утакмица између ширења тау-а и онога што се догодило са мозгом у наредној години била је заиста запањујућа“, рекли су неуролог Гил Рабиновици, др. Мед., Едвард Феин и угледни професор у памћењу и старењу Пеарл Ландритх, вођа ПЕТ програма за снимање у УЦСФ-ов центар за памћење и старење и виши аутор рада.
„Тау ПЕТ снимање предвиђа не само колику ће атрофију видети, већ и где ће се то догодити. Ова предвиђања су била много моћнија од свега што смо могли да урадимо са другим алаткама за снимање и додали смо доказима да је тау главни покретач болести. "
Истраживачи Алзхеимерове болести дуго су расправљали о релативном значају амилоидних плакова и тау заплета - две врсте погрешно склопљених протеинских кластера виђених у постмортем студијама мозга пацијената, које је први идентификовао немачки истраживач др Алоис Алзхеимер почетком 20. века. Деценијама је доминирао „амилоидни камп“, што је довело до вишеструких напора да се Алзхеимерова болест успори лековима који циљају амилоид, а све са разочаравајућим или мешовитим резултатима.
Многи истраживачи сада поново разматрају протеин тау, некада одбачен као "надгробни споменик" који обележава умируће ћелије, и истражују да ли је тау у ствари важан биолошки покретач болести.
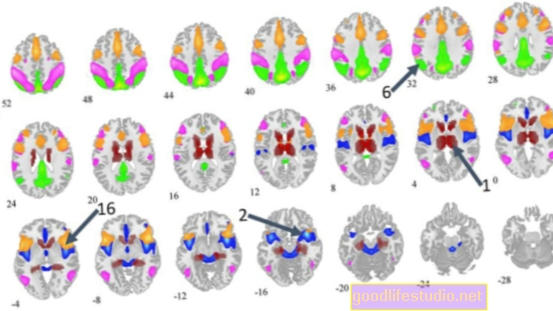
За разлику од амилоида, који се акумулира широм мозга, понекад чак и код људи без симптома, обдукције пацијената са Алзхеимеровом болешћу откриле су да је тау концентрисан управо тамо где је атрофија мозга најтежа и на локацијама које помажу у објашњавању разлика у симптомима пацијената. као на пример у областима везаним за језик у односу на регионе који се односе на меморију.
„Нико не сумња да амилоид игра улогу у Алцхајмеровој болести, али све више и више открића почиње да мења начин на који људи размишљају о томе шта је заправо покретач болести“, објаснио је др Ренауд Ла Јоие, постдокторски истраживач у Рабиновици Ин Виво Молецулар Неуроимагинг Лаб и водећи аутор нове студије. „Ипак, само гледајући постмортално мождано ткиво, било је тешко доказати да тау заплети узрокују дегенерацију мозга, а не обрнуто.
„Један од кључних циљева наше групе био је развити неинвазивне алате за сликање мозга који би нам омогућили да видимо да ли таулу накупина рано у болести предвиђа каснију дегенерацију мозга.“
Упркос раним сумњама да би тау могло бити немогуће измерити у живом мозгу, научници су недавно развили молекул за ињекције назван флортауципир - који тренутно надгледа ФДА - који се везује за погрешно склопљени тау у мозгу и емитује благи радиоактивни сигнал који се може покупити ПЕТ скенирањем.
За студију, Ла Јоие је регрутовао 32 учесника са раном клиничком фазом Алзхеимерове болести путем УЦСФ Центра за памћење и старење, који су сви добили ПЕТ скенирање помоћу два различита трагача за мерење нивоа амилоидног протеина и тау протеина у мозгу. Учесници су такође добили МРИ снимке за мерење структурног интегритета њиховог мозга, како на почетку студије, тако и поново у накнадним посетама годину до две године касније.
Истраживачи су открили да су укупни нивои тау у мозгу учесника на почетку студије предвиђали колика ће се дегенерација догодити до тренутка њихове накнадне посете, у просеку 15 месеци касније. Узорци накупљања тау предвиђали су накнадну атрофију на истим локацијама са више од 40 процената тачности, према налазима студије. Супротно томе, основни амилоид-ПЕТ скенирање тачно је предвидело само 3 процента будуће дегенерације мозга, открили су истраживачи.
„Видети да тау накупљање предвиђа где ће се десити дегенерација подржава нашу хипотезу да је тау кључни покретач неуродегенерације у Алзхеимеровој болести“, рекао је Ла Јоие.
ПЕТ скенирање открило је да су млађи учесници студије имали виши укупни ниво тау у мозгу, као и јачу везу између почетне тау и накнадне атрофије мозга, у поређењу са старијим учесницима. То сугерише да други фактори - вероватно други абнормални протеини или васкуларне повреде - могу играти већу улогу у касном настанку Алзхеимерове болести, кажу истраживачи.
Резултати додају наду да би лекови који циљају тау, а који се тренутно проучавају, могли пружити клиничке користи пацијентима блокирањем овог кључног покретача неуродегенерације у болести. Истовремено, способност употребе тау ПЕТ-а за предвиђање касније дегенерације мозга могла би омогућити персонализовану негу деменције и убрзати текућа клиничка испитивања, према истраживачима.
„Једна од првих ствари које људи желе да знају када чују дијагнозу Алцхајмерове болести је једноставно оно што будућност носи за њих саме или њихове вољене. Да ли ће то бити дуго бледеће памћења или брзи пад у деменцију? Колико дуго ће пацијент моћи самостално да живи? Да ли ће изгубити способност да говоре или се сами сналазе? То су питања на која тренутно не можемо одговорити, осим најопштије, “рекао је Рабиновићи. „По први пут, овај алат би нам могао пружити пацијентима осећај шта могу очекивати откривањем биолошког процеса у основи њихове болести.“
Истраживачи су рекли да такође предвиђају да ће способност предвиђања будуће атрофије мозга на основу тау ПЕТ снимања омогућити Алзхеимер-овим клиничким испитивањима да брзо процене да ли експериментални третман може изменити специфичну путању предвиђену за појединог пацијента, што је тренутно немогуће због широке варијабилност у начину напредовања болести од појединца до појединца.Такви увиди би могли да омогуће прилагођавање дозирања или прелазак на друго експериментално једињење ако први третман не утиче на ниво тау или мења предвиђену путању атрофије мозга код пацијента, објашњавају они.
„Тау ПЕТ могао би бити изузетно драгоцен алат прецизне медицине за будућа клиничка испитивања“, рекао је Рабиновици. „Способност осетљивог праћења накупљања тау код живих пацијената по први пут би клиничким истраживачима омогућила да траже третмане који могу успорити или чак спречити специфични образац атрофије мозга предвиђен за сваког пацијента.“
Студија је објављена у Наука Транслациона медицина.
Извор: Универзитет Калифорнија, Сан Франциско (УЦСФ)
Фото: