Електрична стимулација пружа наду људима с тешким повредама кичмене мождине
Електрична стимулација даје нову наду људима који имају озбиљне повреде кичмене мождине. Студија показује да су четворица младића са параплегијом сада у стању да самостално померају ноге уз помоћ електричне стимулације кичме. Истраживачи верују да терапија има потенцијал да промени прогнозу људи са парализом чак и годинама након повреде.

Откриће „нуди нову перспективу да кичмена мождина, чак и након тешке повреде, има велики потенцијал за функционални опоравак.“ Извор фотографија: 123РФ.цом.
Мушкарци, који су били парализовани више од две године, били су у стању да флексирају ножне прсте, глежњеве и колена користећи електричну стимулацију. Још веће побољшање кретања нађено је када су мушкарци стимулацију користили у комбинацији са физичком рехабилитацијом. Детаљи о овом револуционарном открићу објављени су у часопису Браин .Откриће „нуди нову перспективу да кичмена мождина, чак и након тешке повреде, има велики потенцијал за функционални опоравак“, рекла је главна истражитељица, др. Сц. Истраживачки центар за повреде кичмене мождине у Кентуцкију на универзитету у Лоуисвиллеу (КСЦИРЦ).

Кент Степхенсон, друга особа која је подвргнута епидуралној стимулацији кичмене мождине, добровољно подиже ногу док је стимулатор активан. Фотографија љубазношћу Универзитета у Лоуисвиллеу.
Како дјелује електрична стимулација
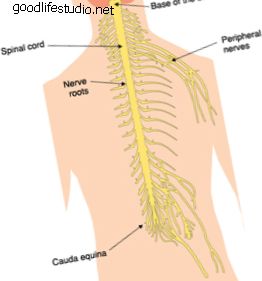
Електрична стимулација укључује импулсе електричне енергије који се шаљу низ кичму како би опонашали сигнале које мозак обично шаље да покрене покрет. Електрични импулси се достављају путем стимулатора који се хируршки поставља на кичмену мождину.
Роб Суммерс, који је парализован испод груди, био је прва особа која је имала користи од овог лечења. Примио је електричне импулсе у кичменој мождини одмах испод повреде, док је свакодневно био подвргнут тренинзима у којима је био суспендован у појасу преко траке, док су му истраживачи помагали да стоји или хода. На крају је Роб могао да стоји сам 4 минута. Седам месеци суђења, Роб је поново стекао добровољну контролу над својим ногама.
Сви мушкарци били су у могућности да синхронизују покрете ногу, глежња и ножних прстију у комбинацији са визуелним знаком успона и падања таласа приказаног на екрану рачунара, а троје од четворо су могли да промене силу којом су се савијали ногу, зависно од интензитета три различите слушне функције.
„Чињеница да је мозак у стању да искористи неколико веза које могу остати, а затим да обради ове компликоване визуелне, слушне и перцептивне информације, прилично је невероватна. То нам говори да информације из мозга стижу на право место у кичмени мождини, тако да особа може да контролише, са прилично импресивном тачношћу, природу покрета ", рекао је др. Реггие Едгертон, одговорни истраживач за развој овог приступа терапији. Др Едгертон је угледни професор за интегративну биологију, физиологију, неуробиологију и неурохирургију на Калифорнијском универзитету у Лос Анђелесу.
Остала побољшања здравља
Сва четворица мушкараца била су у стању самостално да носе тежину, а такође су показала и другачија здравствена побољшања, попут повећане мишићне масе, мање умора и већег осећаја благостања. Роб је, на пример, Роб почео да има бољу контролу крвног притиска, регулацију телесне температуре, контролу мокраћног бешика и сексуалну функцију.
Истраживачи проучавају да ли се епидурална стимулација може користити за помоћ људима који имају парализу руку и развијају технологију за испоруку спиналне стимулације кроз кожу, уместо да хируршки имплантирају стимулатор. Поред тога, истраживачи раде на унапређењу технологије електричних стимулатора како би се постигла већа контрола кретања код људи који имају парализу.
Коментар
Аутор др. Нарихито Нагосхи и Мицхаел Г Фехлингс
У последње време, велика пажња је усмерена на терапијске стратегије за повреду кичмене мождине (СЦИ), укључујући ћелијску трансплантацију и / или примену лекова. Клиничка испитивања неуронских прекурсорских ћелија за СЦИ већ су обављена 1, као и испитивања мезенхималних матичних ћелија 1 и лекова као што су антагонисти натријум / глутамата 2 и антибиотика миноциклин 3 . У том контексту, рад који су Ангели и његове колеге представили у актуелном броју Браин представља нову стратегију за лечење СЦИ 4 . У њихову студију су укључена 4 пацијента са комплетним моторним СЦИ. Више од две године је прошло од СЦИ код свих пацијената, а нивои повреда су се кретали од Ц7 до Т5. Јединице за стимулацију кичмене мождине су хируршки имплантиране на нивоу Т11 / 12. Изненађујуће, сва 4 пацијента са хроничном потпуном парализом поново су добровољно покренула ноге епидуралном стимулацијом убрзо након имплантације уређаја. Штавише, пацијенти би могли активирати моторичко кретање ногу према визуелним и слушним сигналима. Понављајући стојећи и добровољни тренинги помоћу епидуралне стимулације подстакли су већу генерисање силе и тачност покрета мишића ногу.
Упечатљива тачка ове студије је да се терапијска стратегија за СЦИ није усмерила на само место лезије, већ испод нивоа места лезије на кичменој мождини. У терапији ћелијским трансплантацијама фокус је на замјени оштећених неуронских ћелија и промоцији регенерације и ремиелинације аксона на и преко места лезије. Међутим, резултати овог рада демонстрирају нову стратегију активирања поштеђеног круга кичмене мождине испод нивоа повреде епидуралном стимулацијом, без икаквог директног третмана места лезије. У ледвеној кичменој мождини се зна да постоје централни генератори узорка (ЦПГ) који контролирају локомоторно понашање стражњих ногу 5, а епидурална стимулација у овом раду могла би допринети реактивацији ЦПГ неуронског круга. Насупрот томе, остаје механизам помоћу којег се визуелни и слушни улази спуштају у кичмену структуру преко високо поремећених аксона на месту лезије. Међутим, Цоуртине и његове колеге показали су да, без икаквог супраспиналног уноса, механизми учења који зависе од употребе могу промовисати опоравак пуног кретања теретних путева у моделу СЦИ 6 глодара. Стога би стимулација неуронског круга ЦПГ у лумбалној кичмени мождини могла бити нова терапијска мета за СЦИ.
Главно ограничење овог рада је мали број уписаних пацијената. Иако су пацијенти релативно млади (просјечно 26, 9 година), преваленца СЦИ има тенденцију пораста код геријатријских пацијената 7, а исходе у овој групи болесника треба испитати. Будуће студије ће бити потребне за испитивање функционалних ефеката епидуралне стимулације и тренинга у већим клиничким испитивањима.
Погледајте извореАнгели ЦА, Едгертон ВР, Герасименко ИП, Харкема СЈ. Мозак . 2014. дои: 10.1093 / браин / аву038.
Национални институти здравља. Спинална стимулација помаже четверо пацијената с параплегијом да се поврате добровољно. хттп://ввв.них.гов/невс/хеалтх/апр2014/нибиб-08.хтм. Приступљено 8. априла 2014.
Универзитет у Лоуисвиллеу. Четири параплегична мушкарца добровољно померају ноге, што је "невиђени пробој" за заједницу парализе. хттп://лоуисвилле.еду/медицине/невс/фоур-параплегиц-мен-волунтарили-мове-тхеир-легс-ан-унпрецедентед-бреактхроугх-фор-паралисис-цоммунити. Приступљено 8. априла 2014.
Коментар референце
1. Тетзлафф В, ет ал. Систематски преглед терапија ћелијских трансплантација за повреде кичмене мождине. Ј Неуротраума . 28: 1611-1682, дои: 10.1089 / неу.2009.1177 (2011).
2. Фехлингс МГ и др. Рилузол за лечење акутне трауматске повреде кичмене мождине: образложење и дизајн клиничког испитивања НАЦТН фазе И. Ј Неуросург кичме . 17: 151-156, дои: 10.3171 / 2012.4.АОСПИНЕ1259 (2012).
3. Цасха С, ет ал. Резултати рандомизираног испитивања миноциклина у фази акутне повреде кичмене мождине фазе ИИ. Мозак . 135: 1224-1236, дои: 10.1093 / браин / авс072авс072 [пии] (2012).
4. Ангели ЦА, Едгертон ВР, Герасименко ИП, Харкема СЈ. Промјена ексцитабилности кичмене мождине омогућава добровољна кретања након хроничне потпуне парализе код људи. Мозак . дои: аву038 [пии] 10.1093 / браин / аву038 (2014).
5. Киехн О. Локомоторни кругови у кичменој мождини сисара. Анну Рев Неуросци . 29: 279-306, дои: 10.1146 / аннурев.неуро.29.051605.112910 (2006).
6. Цоуртине Г и др. Трансформација нефункционалних кичмених кругова у функционална стања након губитка уноса мозга. Нат Неуросци . 12: 1333-1342, дои: 10.1038 / нн.2401нн.2401 [пии] (2009).
7. Мартин НД, ет ал. Тачка морлета смртности за доб и акутне повреде грлића материце. Ј Траума . 71: 380-385; дискусија 385-386, дои: 10.1097 / ТА.0б013е318228221ф00005373-201108000-00016 [пии] (2011).